腫瘍微小環境における薬剤耐性機構の解明 (担当:倉田)
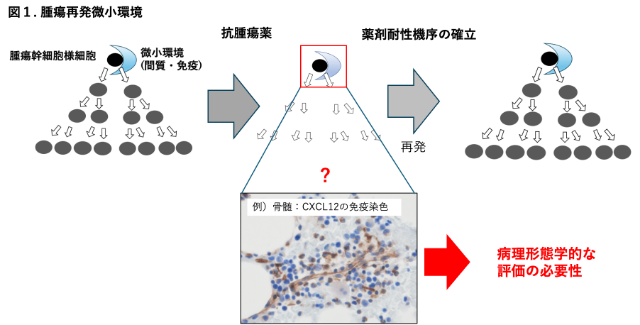
分子標的薬や免疫チェックポイント阻害薬などの抗腫瘍薬は、科学の進歩とともに飛躍的な発展を遂げてきました。しかしながら、がんの再発はいまだ克服すべき大きな課題です。再発の背景には、がん細胞の幹細胞様機能を維持する「腫瘍微小環境」が存在し、微小残存病変の温床として重要な役割を果たしていることが知られています(図1)。
私たちは病理医の立場から、腫瘍微小環境を分子学的・形態学的に“可視化”することを目指しています。それにより、生物学的理解を深化させるだけでなく、新たな治療標的の同定や、「難治性微小環境を有する腫瘍」という新たな疾患概念の確立につなげたいと考えています。
私たちは病理医の立場から、腫瘍微小環境を分子学的・形態学的に“可視化”することを目指しています。それにより、生物学的理解を深化させるだけでなく、新たな治療標的の同定や、「難治性微小環境を有する腫瘍」という新たな疾患概念の確立につなげたいと考えています。
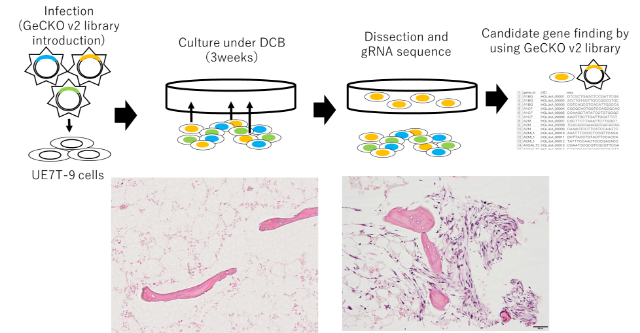
さらに、より本質的な分子機構の解明を目指し、ランダム変異スクリーニングであるIndirect CRISPR screening(図2)を導入しています。機能解析と網羅的発現解析を組み合わせて腫瘍微小環境関連マーカーを抽出・検証し、最終的には病理形態学的手法によって幹細胞と腫瘍微小環境を統合的に可視化することを目標としています。

その他
がん遺伝子変異(RAS, MYCなど)と細胞内シグナルなど、がん生物学に全般にも興味を持って研究を行っています。「なぜ」を大切にして、一緒に研究したい方は是非ご連絡ください。
脱細胞化骨を用いた、新たなヒト骨髄微小環境モデルの開発(担当:大西)
骨髄では、微小な環境下で造血幹細胞と間葉系幹細胞が、相互に関係し合うことで、造血幹細胞の分化と増殖、ひいては造血が維持、制御されています。
間葉系幹細胞の遺伝子変異により、急性白血病や骨髄異形成腫瘍の発生が、マウス実験では示唆されているものの、ヒトのモデルの構築は困難です。
ブタの骨を静水圧にて脱細胞した、脱細胞化骨は、ラットの皮下に移植することで、ラットの造血幹細胞と間葉系幹細胞を誘導し、脱細胞化骨内で造血を誘導することが可能です。我々は、CRISPR screeningによって、ヒトの骨髄間葉幹細胞株を脱細胞化骨内に誘導し、その因子の同定に成功しました。
ヒト間葉幹細胞株を導入した脱細胞化骨を皮下移植することにより、ヒト骨髄造血モデルの構築を目指しています。
間葉系幹細胞の遺伝子変異により、急性白血病や骨髄異形成腫瘍の発生が、マウス実験では示唆されているものの、ヒトのモデルの構築は困難です。
ブタの骨を静水圧にて脱細胞した、脱細胞化骨は、ラットの皮下に移植することで、ラットの造血幹細胞と間葉系幹細胞を誘導し、脱細胞化骨内で造血を誘導することが可能です。我々は、CRISPR screeningによって、ヒトの骨髄間葉幹細胞株を脱細胞化骨内に誘導し、その因子の同定に成功しました。
ヒト間葉幹細胞株を導入した脱細胞化骨を皮下移植することにより、ヒト骨髄造血モデルの構築を目指しています。
CRISPR Screening databaseを用いた、新たな癌治療標的の探索(担当:大西)
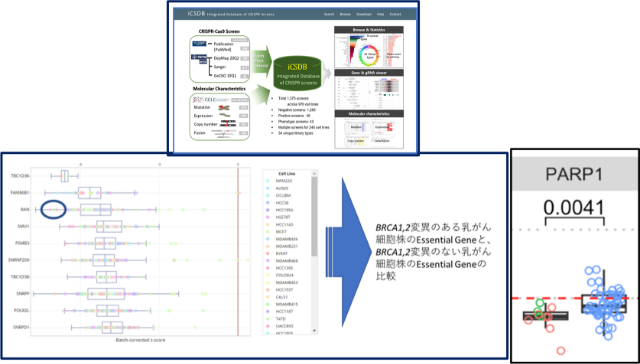
大規模なCRISPR Scrreeningの実施により、主な細胞株の生存に必要な遺伝子(Essential gene)がデータベース化され、無償で閲覧可能です。iCSDBというデータベース(https://academic.oup.com/nar/article/49/D1/D956/5952197)では、細胞株ごとに、Essential geneを参照できることから、データベース上で遺伝子変異に対応するようなessential geneの特定、ひいては治療標的を発見できるのではないかと考えております。私は、BRCA変異乳癌において、近年有効性が確認されているPARP阻害薬に代わるような治療標的をデータベース上で同定し、その確認実験を行なっています。
その他
「好きこそものの上手なれ」、好きな研究テーマを楽しんで取り組み、研究をレベルアップさせていければ最高です。
是非一緒に、好きな研究に取り組みましょう。
腫瘍微小環境を標的とした口腔扁平上皮癌の新規治療戦略の検討(担当:關)
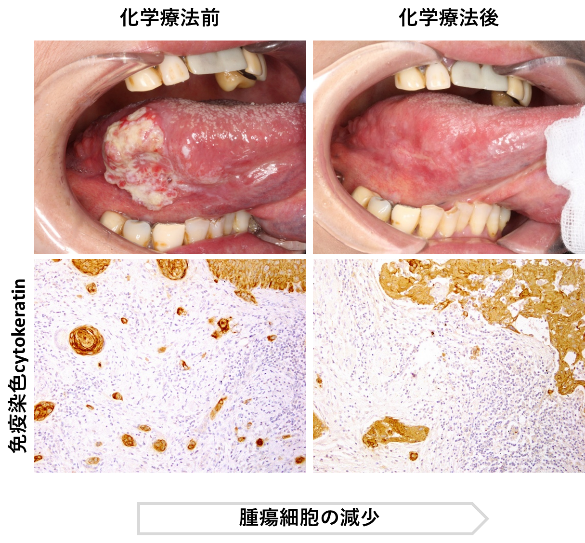
口腔扁平上皮癌は、早期に発見されれば外科的手術によって治癒が期待できる腫瘍です。しかし、悪性度の高い症例では頸部リンパ節や肺への転移を起こすことがあり、その場合は予後が不良になることがあります。そのような症例に対しては、これまで術前・術後の化学療法や放射線療法が行われてきましたが、それでも救済できない悪性度の高い症例があります。右写真は、術前化学療法を行った症例で、腫瘍が縮小し、免疫染色(cytokeratin)でも一部の腫瘍細胞は壊死し、腫瘍の量も減っているのが確認できます。近年では免疫療法も新たな治療の選択肢として注目されており、これらの治療を組み合わせることにより、予後改善が期待されます。
私たちは、腫瘍そのものだけでなく、腫瘍の周囲に存在する免疫細胞などから構成される「腫瘍微小環境」に注目して研究を行っています。腫瘍微小環境は、腫瘍の増殖や浸潤、転移に深く関わっていると考えられており、この環境を標的とすることで新しい治療戦略の開発につながる可能性があります。
また、治療方針を決定するうえでは、手術前に行う生検で腫瘍の悪性度を正確に評価することが重要です。そのため、生検標本から腫瘍の悪性度をどこまで評価できるか、さらに腫瘍細胞とその周囲の微小環境との関係についても研究しています。これにより、患者さん一人ひとりに適した個別化治療の実現を目指しています。
私たちは、腫瘍そのものだけでなく、腫瘍の周囲に存在する免疫細胞などから構成される「腫瘍微小環境」に注目して研究を行っています。腫瘍微小環境は、腫瘍の増殖や浸潤、転移に深く関わっていると考えられており、この環境を標的とすることで新しい治療戦略の開発につながる可能性があります。
また、治療方針を決定するうえでは、手術前に行う生検で腫瘍の悪性度を正確に評価することが重要です。そのため、生検標本から腫瘍の悪性度をどこまで評価できるか、さらに腫瘍細胞とその周囲の微小環境との関係についても研究しています。これにより、患者さん一人ひとりに適した個別化治療の実現を目指しています。
その他
さらに、口腔領域には歯原性腫瘍などの腫瘍も存在するため、これらの病変を対象とした病理学的研究も行っています。口腔の病気を病理学的に解明することに興味があり、将来歯科医師として口腔病理医を目指す学生の皆さんの参加を歓迎しています。
肺癌の進展機構の解明と、他疾患との鑑別を目指して(担当:杉田)
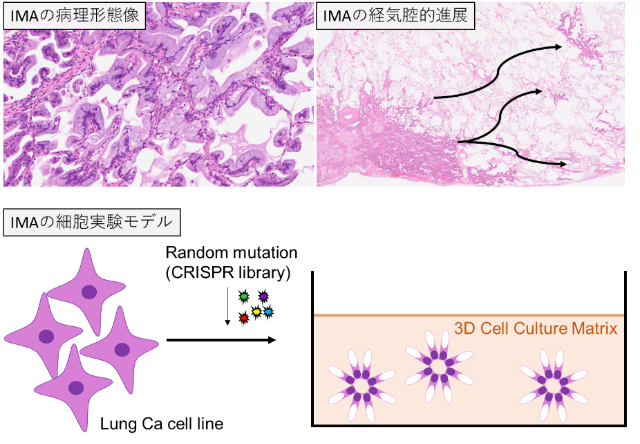
肺癌は日本において最も死亡数の多いがんであり、その進展機構の理解は重要な医学的課題です。私たちは肺癌の中でも特殊なタイプである「肺浸潤性粘液性腺癌(IMA)」に興味を持っています。この腫瘍は、腫瘍細胞が粘液を豊富に産生し、肺胞の空間を介して広がるという特徴的な進展様式を示します。病理診断の現場では、腫瘍細胞が粘液中に浮遊しながら肺内に広がっていく像が観察されますが、この現象がどのような分子機構によって成立しているのかは、まだ十分に解明されていません。
そこで、私たちは腫瘍細胞が「粘液に富む肺胞腔内」という特殊な微小環境にどのように適応し、生存・移動・再定着するのかという点に注目しています。培養細胞モデルや遺伝子解析技術を用い、このような腫瘍進展を可能にする分子機構の解明を目指しています。
また、病理診断上の重要な課題として、IMAと膵癌など他臓器の粘液産生腫瘍の肺転移は形態学的に類似することがあり、その鑑別が問題となる場合があります。私たちは、このような腫瘍の鑑別に役立つ病理形態学的・分子生物学的指標の探索にも取り組んでいます。
そこで、私たちは腫瘍細胞が「粘液に富む肺胞腔内」という特殊な微小環境にどのように適応し、生存・移動・再定着するのかという点に注目しています。培養細胞モデルや遺伝子解析技術を用い、このような腫瘍進展を可能にする分子機構の解明を目指しています。
また、病理診断上の重要な課題として、IMAと膵癌など他臓器の粘液産生腫瘍の肺転移は形態学的に類似することがあり、その鑑別が問題となる場合があります。私たちは、このような腫瘍の鑑別に役立つ病理形態学的・分子生物学的指標の探索にも取り組んでいます。
その他
病理学は基礎医学と臨床医学の橋渡しとなる学問であり、疾患の形態学的観察から出発して分子レベルの理解へと発展していきます。私たちは、病理診断で得られる知見を出発点として腫瘍の生物学的メカニズムを探求したいと考えています。大きな目標を胸に、楽しく実験できればと思っています。ご興味のある方はぜひお気軽にご連絡ください。
